
Contacto:Error Zhou (Señor.)
Teléfono: más 86-551-65523315
Móvil/WhatsApp: más 86 17705606359
QQ:196299583
Skype:lucytoday@hotmail.com
Correo electrónico:sales@homesunshinepharma.com
Agregar:1002, Huanmao edificio, Nº 105, Mengcheng camino, hefei ciudad, 230061, Porcelana
Sanofi anunció recientemente los resultados positivos del estudio COMET Fase III cabeza a cabeza de la terapia de reemplazo enzimático (ERT) avalglucosidasa alfa (neoGAA). Los datos mostraron que el medicamento mostró mejoras clínicamente significativas en las manifestaciones clave de la enfermedad de Pompe de inicio tardío (LOPD) (respiración desordenada y disminución de la movilidad). El estudio también alcanzó el objetivo primario: en pacientes con LOPD, la avalglucosidasa alfa mostró no inferioridad en la mejora de la función respiratoria en comparación con el fármaco estándar de atención Lumizyme (alglucosidasa alfa, aglucosidasa alfa). Estos datos formarán la base para la presentación regulatoria global esperada en la segunda mitad de este año. Anteriormente, la FDA de EE. UU. Había otorgado avalglucosidasa alfa para la calificación avanzada de medicamentos (BTD) y la calificación de vía rápida (FTD) para el tratamiento de la enfermedad de Pompe.
COMET es un estudio aleatorizado, doble ciego, de fase III frente a frente que inscribió a 100 niños y adultos con LOPD que no habían recibido tratamiento previamente en 56 centros en 20 países. En el estudio, estos pacientes se dividieron aleatoriamente en dos grupos y recibieron una infusión intravenosa de 20 mg / kg de avalglucosidasa alfa o 20 mg / kg de aglucosidasa alfa (atención estándar) cada 2 semanas durante 49 semanas. Después de 49 semanas, los pacientes que recibieron atención estándar cambiaron a tratamiento abierto con avalglucosidasa alfa a 20 mg / kg. El objetivo principal del estudio fue: el porcentaje de capacidad vital forzada (FVC) predicho en posición vertical para evaluar los cambios en la función muscular respiratoria.
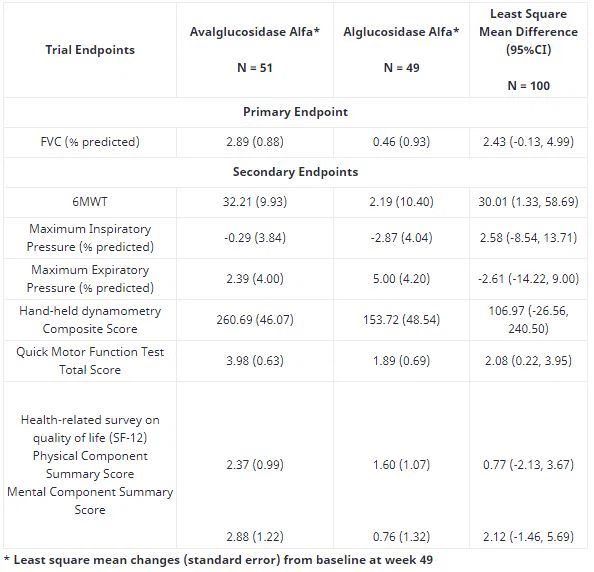
Los datos muestran que, en comparación con los medicamentos de atención estándar (IC 95%, -0.13 / 4.99), el porcentaje de FVC predicho por los pacientes que recibieron avalglucosidasa alfa aumentó en 2.4 puntos porcentuales, y la mejora numérica en la función respiratoria excedió la no inferioridad del diseño del estudio. Índice (p=0,0074).
El criterio de valoración primario también midió la superioridad, mostrando que la ventaja de la avalglucosidasa alfa no fue estadísticamente significativa (p=0.0626). Por lo tanto, de acuerdo con el sistema jerárquico del programa de investigación, no existe una prueba estadística formal para todos los puntos finales secundarios.
Un criterio de valoración secundario clave en este estudio fue la prueba de caminata de 6 minutos (6MWT) para medir la movilidad. Los pacientes tratados con avalglucosidasa alfa tuvieron una distancia de 30 metros más que los pacientes que recibieron medicación de atención estándar (IC 95%: 1.33-58.69). Otros puntos finales secundarios evaluaron la fuerza muscular respiratoria, la función motora y la calidad de vida.
Además, un análisis preliminar preespecificado evaluó el porcentaje predicho de FVC y 6MWT entre los pacientes que cambiaron de medicación de cuidado estándar al tratamiento con avalglucosidasa alfa en la semana 49 durante el período de expansión abierto del estudio. Debido a la inscripción secuencial, en el punto de tiempo de análisis inicial: 97 semanas, 20 de 49 pacientes convertidos habían pronosticado datos de porcentaje de FVC y 21 pacientes tenían datos de 6MWT. Entre estos pacientes convertidos, la avalglucosidasa alfa mostró una mejora de la CVF (IC 95%: -1.95 / 2.25) en 0.15 puntos y 6MWT (IC 95%: -3.87 / 50.51) en 23.32 metros.
La seguridad de la avalglucosidasa alfa es comparable a la de los medicamentos de atención estándar. Durante el período doble ciego de 49 semanas, 44 pacientes en el grupo de avalglucosidasa alfa y 45 pacientes en el grupo de atención estándar experimentaron eventos adversos (EA). Hubo 6 eventos adversos graves en el grupo de avalglucosidasa alfa y 7 en el grupo de tratamiento estándar. Hubo menos pacientes con eventos adversos graves (SAE) en el grupo de avalidasa alfa (8 pacientes, incluido 1 posible SAE relacionado con el tratamiento) que en el grupo de atención estándar (12 pacientes, incluidos 3 posibles SAE relacionados con el tratamiento).
En el grupo de atención estándar, 4 pacientes tuvieron eventos adversos que llevaron a la interrupción del estudio, y 1 paciente murió por un evento adverso de infarto agudo de miocardio (no relacionado con el tratamiento). En el grupo de avalglucosidasa alfa, ningún paciente interrumpió o falleció. El grupo de avalglucosidasa alfa (25.5%) tuvo al menos una reacción relacionada con la perfusión definida por el protocolo que el grupo de atención estándar (32.7%). Los datos de inmunogenicidad se están analizando actualmente y se anunciarán en una futura conferencia médica.
El Dr. Jordi Díaz-Manera, profesor de Enfermedades Neuromusculares, Medicina Traslacional y Genética, Centro de Investigación de Distrofia Muscular John Walton, Universidad de Newcastle, Reino Unido, dijo:&"; la enfermedad de Pompeya deteriorará gradualmente los músculos y debilitará a las personas. Es importante destacar el potencial El nuevo régimen de tratamiento permitirá a los pacientes lograr mejoras clínicamente significativas en múltiples mediciones de la función respiratoria y motora. Los resultados del estudio de fase III COMET son muy alentadores, y se ha agregado cada vez más evidencia clínica para demostrar que la avalglucosidasa alfa es el potencial para proporcionar nuevas opciones de tratamiento para abordar los síntomas característicos de esta enfermedad."
El Dr. John Reed, director global de investigación y desarrollo de Sanofi, dijo: "Estamos contentos de que la avalglucosidasa alfa haya mostrado mejoras clínicamente significativas en la función y actividad respiratoria, según lo medido por los indicadores de pronóstico estándar aceptados de la enfermedad de Pompe. Estos resultados subrayan nuestra ambición de usar avalglucosidasa alfa como un nuevo estándar de atención para la enfermedad de Pompe."

Camino de Pompeya (Fuente de la imagen: foodnhealth.org)
La enfermedad de Pompe es causada por defectos genéticos o disfunción de la enzima alfa-glucosidasa ácida lisosomal (GAA), lo que resulta en la acumulación de glucógeno en los músculos (incluidos los músculos proximales y el diafragma), lo que finalmente conduce a un daño muscular progresivo e irreversible. Esta enfermedad rara afecta a aproximadamente 50,000 personas en todo el mundo y puede manifestarse a cualquier edad desde bebés hasta la edad adulta tardía. La enfermedad de Pompeya generalmente se clasifica como enfermedad de Pompe de inicio tardío (LOPD) o enfermedad de Pompe infantil (IOPD). Los pacientes con LOPD generalmente aparecen desde el primer año de vida hasta la edad adulta tardía. Los síntomas característicos de la LOPD son la función respiratoria deteriorada y la debilidad del músculo esquelético, lo que a menudo resulta en una capacidad de ejercicio deteriorada. Los pacientes generalmente necesitan una silla de ruedas para moverse, o pueden necesitar ventilación mecánica para respirar. La insuficiencia respiratoria es la causa más común de muerte en pacientes con enfermedad de Pompe. Cuando la enfermedad de Pompe se clasifica como IOPD, los síntomas comienzan a aparecer antes de la edad de uno. Además de la debilidad del músculo esquelético, la función cardíaca también se ve afectada en general.
El propósito de la terapia de reemplazo de enzimas (ERT) de Pompeya&es introducir enzimas (GAA) en los lisosomas en las células musculares para reemplazar los GAA faltantes o faltantes. GAA es una enzima necesaria para prevenir la acumulación de glucógeno en el músculo. La avaloglucosidasa alfa es un ERT de la enfermedad de Pompe en desarrollo, cuyo objetivo es mejorar el suministro de enzimas a las células musculares, especialmente al músculo esquelético. En comparación con el medicamento de atención estándar alglucosidasa alfa (Aglucosidasa alfa), el contenido de manosa-6-fosfato (M6P) de avaloglucosidasa alfa aumenta aproximadamente 15 veces, el objetivo es ayudar a aumentar la absorción de enzimas celulares y el glucógeno en los tejidos objetivo Claro. La relevancia clínica de esta diferencia no ha sido confirmada.
Lumizyme (glucosidasa alfa) es el ERT de primera generación desarrollado por Sanofi y ha sido aprobado para el tratamiento de la enfermedad de Pompe. La avaloglucosidasa alfa es un ERT de glucosidasa alfa (alglucosidasa alfa) de segunda generación, diseñado específicamente para mejorar la focalización del receptor y la absorción de enzimas para mejorar el aclaramiento de glucógeno mediante una mayor afinidad por los receptores M6P en las células musculares y mejorar la eficacia clínica de la glucosidasa α. En estudios preclínicos, la avaloglucosidasa alfa mostró aproximadamente 5 veces la eficacia de la aglucosidasa α para reducir el glucógeno tisular. En un modelo de ratón de la enfermedad de Pompe, la avaloglucosidasa alfa mostró un nivel similar de reducción del sustrato con una quinta dosis de aglucosidasa alfa.