
Contacto:Error Zhou (Señor.)
Teléfono: más 86-551-65523315
Móvil/WhatsApp: más 86 17705606359
QQ:196299583
Skype:lucytoday@hotmail.com
Correo electrónico:sales@homesunshinepharma.com
Agregar:1002, Huanmao edificio, Nº 105, Mengcheng camino, hefei ciudad, 230061, Porcelana
Eli Lilly anunció recientemente que los resultados detallados del ensayo clínico de fase 3 SURPASS-4 (NCT03730662) que evalúa la tirzepatida (LY3298176) agonista del receptor de doble acción GIP y GLP-1 para el tratamiento de la diabetes tipo 2 se han publicado en las principales revistas médicas internacionales." The Lancet" (La lanceta). Para obtener más información, ver: Tirzepatida versus insulina glargina en la diabetes tipo 2 y aumento del riesgo cardiovascular (SURPASS-4): un ensayo de fase 3 aleatorizado, abierto, de grupos paralelos, multicéntrico.
Los datos muestran que en pacientes adultos con diabetes tipo 2 con mayor riesgo cardiovascular (CV), en comparación con insulina glargina titulada, las tres dosis de tirzepatida muestran superioridad en la reducción del azúcar en sangre y el peso corporal: tratamiento durante 52 semanas, con efecto curativo Estimación (eficacia estimar) método de análisis estadístico, la dosis más alta de tirzepatida (15 mg, una vez a la semana) reduce el nivel de glucosa en sangre (A1C) desde el valor inicial en un 2,58% y el peso desde el valor inicial en 11,7 kg (25,8 libras, 13,0%) y la titulación de insulina. glargina redujo la A1C desde el valor inicial en un 1,44% y el peso corporal aumentó en 1,9 kg (4,2 libras, 2,2%) desde el valor inicial.
SURPASS-4 es el ensayo más grande y más largo del proyecto SURPASS hasta el momento, y también es el quinto y último estudio de registro global completado sobre tirzepatida para el tratamiento de la diabetes tipo 2. El criterio de valoración principal se midió a las 52 semanas y los pacientes continuaron el tratamiento durante 104 semanas o hasta que se completó el estudio. La finalización del estudio fue provocada por la acumulación de eventos cardiovasculares adversos mayores (MACE) para evaluar el riesgo de CV. En los datos publicados recientemente para el período de tratamiento después de 52 semanas, los pacientes tratados con tirzepatida mantuvieron la A1C y el control del peso hasta por 2 años.
La seguridad general de tirzepatida evaluada durante todo el período del estudio fue consistente con los resultados de seguridad medidos durante 52 semanas, y no hubo nuevos hallazgos durante 104 semanas. Los efectos secundarios gastrointestinales son los eventos adversos más comunes, que generalmente ocurren durante el período de aumento de la dosis y luego disminuyen con el tiempo.
La tirzepatida es un nuevo tipo de polipéptido insulinotrópico dependiente de glucosa (GIP, también conocido como polipéptido inhibidor gástrico) y de activación dual del receptor del péptido 1 similar al glucagón (GLP-1) desarrollado por Eli Lilly. Agente. Tanto GIP como GLP-1 son hormonas secretadas por el tracto intestinal, que pueden promover la secreción de insulina. La tirzepatida integra los efectos de dos efectos promotores de la insulina en una sola molécula y representa una nueva clase de medicamentos para el tratamiento de la diabetes tipo 2.
El proyecto de desarrollo clínico global SURPASS Phase 3 ha inscrito a más de 13.000 pacientes con diabetes tipo 2 en 10 ensayos clínicos, 5 de los cuales son estudios de registro global. El proyecto se lanzó a fines de 2018 y se completaron las cinco pruebas de registro global.
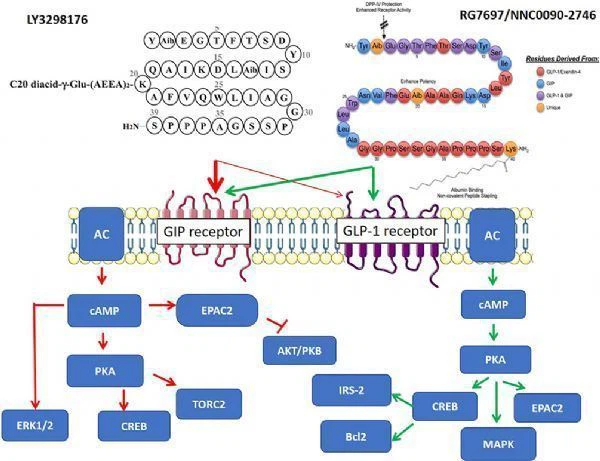
tirzepatide (LY3298176, imagen de la literatura: PMID-31686879)
SURPASS-4 es un ensayo global de etiqueta abierta, en 2002 casos de aumento de riesgo cardiovascular (CV), han recibido 1-3 fármacos hipoglucemiantes orales (metformina, sulfonilurea, inhibidores de SGLT2) tratamiento pero los niveles de azúcar en sangre están controlados Se realizó en adultos con diabetes tipo 2 deficiente, y se evaluó la eficacia y seguridad de tres dosis de tirzepatida (5 mg, 10 mg, 15 mg) e insulina glargina titulada. Entre todos los pacientes aleatorizados, 1.819 (91%) completaron el seguimiento inicial de 52 semanas y 1706 (85%) completaron el tratamiento del estudio. La duración media del estudio fue de 85 semanas y 202 pacientes (10%) completaron el estudio de 2 años.
En el estudio, la duración media de la diabetes fue de 11,8 años, la A1C inicial fue del 8,52%, el peso inicial fue de 90,3 kg y el 85% de los pacientes tenía antecedentes de enfermedad cardiovascular. En el grupo de insulina glargina, la dosis de insulina se tituló de acuerdo con el algoritmo estándar de tratamiento, con el objetivo de que la glucosa en sangre en ayunas fuera inferior a 100 mg / dL. La dosis inicial de insulina glargina es de 10 unidades / día y la dosis promedio de insulina glargina a las 52 semanas es de 43 unidades / día.
En este estudio, se utilizaron dos métodos de estimación (estimación de eficacia [estimación de eficacia] y estimación del plan de tratamiento [estimación de régimen de tratamiento]) para comparar las diferencias de tratamiento. La eficacia estimada se refiere al efecto antes de suspender el fármaco del estudio o iniciar la terapia de rescate para tratar la hiperglucemia grave persistente. La estimación del régimen de tratamiento se refiere a la eficacia del tratamiento de la hiperglucemia grave persistente independientemente de si se adhiere al fármaco del estudio o si se utiliza una terapia de rescate.
Los resultados mostraron que el estudio alcanzó los puntos finales primarios y secundarios clave utilizando los dos métodos de medición: en comparación con la insulina glargina, a las 52 semanas, las tres dosis (5 mg, 10 mg, 15 mg) de tirzepatida redujeron significativamente la glucosa en sangre (A1C) y el peso corporal. y son estadísticamente significativos.
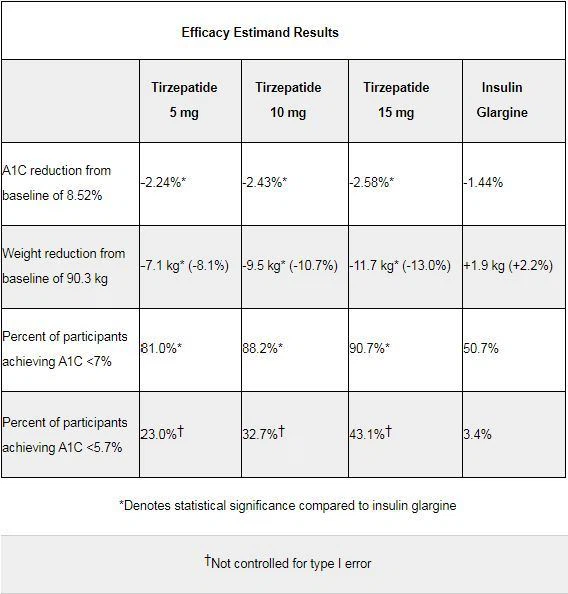
Datos de investigación de SURPASS-4