
Contacto:Error Zhou (Señor.)
Teléfono: más 86-551-65523315
Móvil/WhatsApp: más 86 17705606359
QQ:196299583
Skype:lucytoday@hotmail.com
Correo electrónico:sales@homesunshinepharma.com
Agregar:1002, Huanmao edificio, Nº 105, Mengcheng camino, hefei ciudad, 230061, Porcelana
BioMarin es una empresa global de biotecnología dedicada al desarrollo y comercialización de terapias innovadoras para pacientes con enfermedades genéticas raras y ultrararas graves y potencialmente mortales. Su cartera de productos incluye 6 productos comerciales y una variedad de productos candidatos clínicos y preclínicos. Recientemente, la compañía anunció que la Agencia Europea de Medicamentos (EMA) ha aceptado la solicitud de autorización de comercialización (MAA) para vosoritide (Voxolitide, BMN111).
Vosoritide es un análogo del péptido natriurético (CNP) de tipo C que se inyecta una vez al día para el tratamiento de la acondroplasia infantil, que es la estatura baja desproporcionada más común en humanos. En la Unión Europea, la revisión de MAA comenzó el 13 de agosto. La compañía aún planea enviar una nueva solicitud de fármaco (NDA) para vosoritide a la Administración de Drogas y Alimentos de los Estados Unidos (FDA) en el tercer trimestre de 2020. En la Unión Europea y en los Estados Unidos, a vosoritide se le ha otorgado la Designación de Medicamento Huérfano (ODD) para el tratamiento de la acondroplasia.
Si se aprueba, vosoritide se convertirá en el primer fármaco para tratar la acondroplasia. El medicamento puede tratar la causa raíz de la enfermedad y representa un gran avance médico con el potencial de tener un impacto significativo en los pacientes' vive.
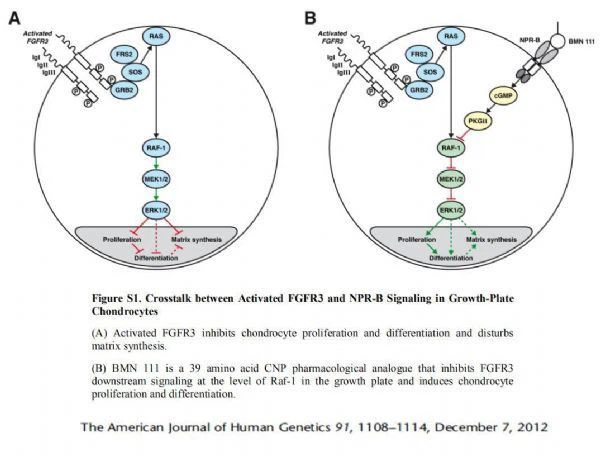
Mecanismo de acción de vosoritide
La acondroplasia es la estatura baja desproporcionada más común en humanos. Se caracteriza por una osificación endocondral más lenta, que conduce a un acortamiento desproporcionado y trastornos estructurales de los huesos largos, la columna, la cara y la base del cráneo. Esta afección es causada por mutaciones en el gen del receptor 3 del factor de crecimiento de fibroblastos (FGFR3), que es un regulador negativo del crecimiento óseo.
Además de una estatura desproporcionadamente baja, los pacientes con acondroplasia pueden experimentar complicaciones de salud graves, como compresión del foramen, apnea del sueño, piernas dobladas, hipoplasia facial, columpios lumbares permanentes, estenosis espinal y orejas recurrentes. Departamento de Infección. Algunas de estas complicaciones pueden resultar en la necesidad de una cirugía invasiva, como descompresión de la médula espinal y enderezamiento de las piernas dobladas. Además, los estudios han demostrado que las tasas de mortalidad están aumentando para cada grupo de edad.
Vosoritide es un análogo del péptido natriurético (CNP) de tipo C derivado de péptidos humanos naturales y es un estimulador eficaz de la osificación endocondral. El péptido humano natural es un regulador positivo del crecimiento óseo. Vosoritide se une a receptores específicos e inicia señales intracelulares que inhiben la vía hiperactiva del FGFR3.

La aplicación reglamentaria de vosoritide se basa en los resultados de un estudio fase III aleatorizado, doble ciego y controlado con placebo, publicado en diciembre de 2019, y además obtiene los datos de seguridad y eficacia a largo plazo de la expansión en curso de fase II y fase III. estudios, datos extensos sobre el historial de enfermedades naturales.
El estudio global de fase III inscribió a 121 niños con acondroplasia que tenían entre 5 y 14 años de edad y cuyas placas de crecimiento aún estaban abiertas, y evaluó la eficacia y seguridad de vosoritide y placebo. Estos pacientes habían completado al menos 6 meses de estudio inicial antes de ingresar al estudio de fase III para determinar sus respectivas tasas de crecimiento inicial. En el estudio de fase III, los pacientes fueron asignados al azar para recibir 52 semanas de vosoritida (15 ug / kg / día) o placebo. El criterio de valoración principal fue el cambio en la tasa de crecimiento desde el inicio en los niños tratados con vosoritide durante el período de tratamiento de un año en comparación con el placebo.
Los resultados mostraron que el estudio alcanzó el criterio de valoración principal: después de un año de tratamiento, el cambio en la tasa de crecimiento del tratamiento con vosoritida desde el inicio fue de 1,6 cm / año (p< 0,0001)="" después="" de="" un="" año="" de="" tratamiento.="" este="" resultado="" es="" consistente="" con="" los="" resultados="" en="" la="" amplia="" población="" de="" pacientes="" estudiada.="" en="" el="" estudio,="" la="" vosoritida="" fue="" generalmente="" bien="" tolerada="" y="" no="" hubo="" una="" caída="" clínicamente="" significativa="" de="" la="" presión="">
Los resultados de un estudio de fase II de descubrimiento de dosis de etiqueta abierta publicado en noviembre de 2019 mostraron que, en comparación con un nuevo conjunto de datos de acondroplasia de historia natural (n=619), los niños que recibieron 15 μg de edad y sexo coincidieron en la cohorte tres (n=10) pacientes tratados con vosoritida / kg / día, la estatura media acumulada aumentó 9,0 cm en 54 meses y los datos fueron estadísticamente significativos (p< 0,005).="" con="" un="" aumento="" de="" 2,2="" cm="" en="" los="" últimos="" 12="" meses,="" los="" datos="" ilustran="" aún="" más="" el="" efecto="" beneficioso="" del="" tratamiento="" continuo="" con="" vosoritida="" sobre="" la="">