
Contacto:Error Zhou (Señor.)
Teléfono: más 86-551-65523315
Móvil/WhatsApp: más 86 17705606359
QQ:196299583
Skype:lucytoday@hotmail.com
Correo electrónico:sales@homesunshinepharma.com
Agregar:1002, Huanmao edificio, Nº 105, Mengcheng camino, hefei ciudad, 230061, Porcelana
AstraZeneca y Merck& Co anunció recientemente que su medicamento contra el cáncer dirigido, Koselugo (selumetinib), ha recibido la aprobación condicional de la Comisión Europea (CE). Este fármaco es un nuevo tipo de inhibidor de la quinasa oral para su uso en 3 años y más1 Los pacientes pediátricos con neurofibromatosis (NF1) tratan los neurofibromas plexiformes (NP) sintomáticos e irresecables. Esta aprobación convierte a Koselugo en el primer fármaco para tratar la NF1 en Europa. Antes de esta aprobación, la cirugía era la única opción de tratamiento para el tratamiento de la NP en niños con NF1 en la UE. Esta aprobación marca un importante paso adelante para abordar los efectos debilitantes de estos tumores.
La NF1 es una enfermedad genética debilitante del sistema nervioso, con una incidencia global de un caso por cada 3.000 personas. En el 30-50% de los pacientes con NF1, el tumor se presenta en la vaina nerviosa (neurofibroma plexiforme [PN1]), lo que puede causar problemas clínicos como: desfiguración, disfunción de las vías respiratorias, deterioro visual, disfunción de la vejiga / intestino.
En abril de 2020, la FDA de EE. UU. Aprobó Koselugo para el tratamiento de neurofibromas plexiformes (NP) sintomáticos e inoperables relacionados con la NF1 en pacientes pediátricos con NF1 de 2 años o más. Cabe mencionar que Koselugo es el primer fármaco aprobado por la FDA de EE. UU. Para el tratamiento de la NF1. Anteriormente, a Koselugo se le concedió la Designación de fármaco huérfano (ODD) y la Designación de fármaco innovador (BTD) para el tratamiento de la NF1. Koselugo es un inhibidor de la quinasa, lo que significa que puede actuar a través de enzimas clave para prevenir el crecimiento de células tumorales.
Esta aprobación se basa en los resultados del ensayo Fase II SPRINT Estrato 1. Este es un ensayo patrocinado por el Proyecto de Evaluación del Tratamiento del Cáncer (CTEP) del Instituto Nacional del Cáncer (NCI). Los resultados relevantes han sido publicados en la principal revista médica internacional" New England Journal of Medicine" (NEJM), ver:selumetiniben niños con plexiforme inoperable.
El ensayo SPRINT Stratum 1 reclutó a 50 pacientes pediátricos (mediana de edad 10,2 años, rango: 3,5-17,4), estos niños tenían NF1 y NP inoperable (definida como resección incompleta pero que no supondría un riesgo grave para el paciente NP). Los síntomas relacionados con los neurofibromas más comunes son desfiguración (44 casos), disfunción motora (33 casos) y dolor (26 casos). En el ensayo, los pacientes tomaron por vía oral 25 mg / m2 (la dosis recomendada aprobada) de Koselugo dos veces al día hasta que la afección empeoró o se produjeron reacciones adversas inaceptables. Durante el ensayo, se evaluaron de forma rutinaria los cambios en el volumen tumoral del paciente y los síntomas de la enfermedad relacionada con el tumor, y se determinó la tasa de respuesta general (TRO), que se definió como una respuesta completa o parcial confirmada por resonancia magnética en 3-6 meses (volumen tumoral NP reducción ≥ 20%) la proporción de pacientes.
Los datos muestran que la monoterapia con Koselugo (por vía oral, dos veces al día) tiene importantes beneficios clínicos para los pacientes: puede reducir continuamente el tamaño del tumor, aliviar el dolor, mejorar la función diaria y la calidad de vida relacionada con la salud en general. En este ensayo, la tasa de respuesta objetiva (TRO) del tratamiento con Koselugo fue del 66% y 33 de 50 pacientes confirmaron respuestas parciales. La TRO se refiere al porcentaje de pacientes con remisión completa (desaparición de NP) o remisión parcial (RP, reducción del volumen tumoral en al menos un 20%).
Los datos de eficacia y seguridad obtenidos del seguimiento más prolongado del ensayo SPRINT Stratum 1 es una de las condiciones para la aprobación condicional de Koselugo por parte de la UE &.
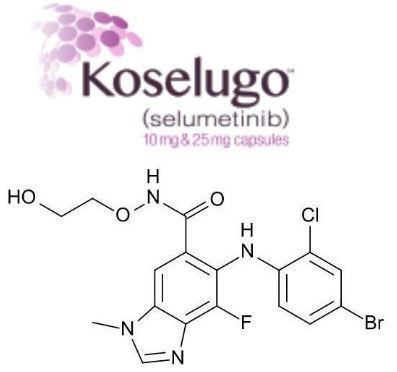
Estructura molecular del ingrediente farmacéutico activo Koselugo selumetinib
La NF1 es una enfermedad poco común que es debilitante, progresiva y, a menudo, desfigura. Esta enfermedad generalmente comienza temprano en la vida y es causada por mutaciones o defectos en genes específicos. La NF1 generalmente se diagnostica en la primera infancia. La NF1 está presente en aproximadamente uno de cada 3.000 bebés, que se caracteriza por cambios en el color de la piel (pigmentación), daño a los nervios y huesos y el riesgo de desarrollar tumores benignos y malignos a lo largo de la vida. El 30% -50% de los pacientes con NF1 tienen uno o más neurofibromas plexiformes (NP). El principal tratamiento de la NP es la resección quirúrgica. Desafortunadamente, debido a la ubicación o el volumen de estos tumores, muchos pacientes no son aptos para la cirugía. Además, la NP suele reaparecer después de una resección quirúrgica óptima y, por lo tanto, representa un área importante de necesidades médicas insatisfechas.
El ingrediente farmacéutico activo de Koselugo esselumetinib, que es un inhibidor de quinasa MEK1 / 2 oral, potente y selectivo. El gen NF1 codifica la neurofibromina (neurofibromina), que regula negativamente la vía RAS / MAPK y ayuda a controlar el crecimiento, la diferenciación y la supervivencia celular. Las mutaciones en el gen NF1 pueden conducir a la desregulación de la vía de señalización RAS / RAF / MEK / ERK, lo que puede hacer que las células crezcan, se dividan y se repliquen de manera descontrolada y pueden conducir al crecimiento tumoral. Selumetinib potencialmente inhibe el crecimiento tumoral al inhibir la enzima MEK en esta vía. Actualmente, selumetinib se está evaluando como una terapia de agente único y se combina con otras terapias para tratar múltiples tipos de tumores en estudios clínicos.
selumetinibfue descubierto por Array BioPharma, y AstraZeneca autorizó los derechos exclusivos mundiales del compuesto en 2003. En julio de 2018, AstraZeneca y Merck llegaron a una cooperación estratégica oncológica para desarrollar y comercializar conjuntamente selumetinib y el inhibidor de PARP Lynparza a escala mundial. Actualmente, las dos partes están llevando a cabo una investigación clínica SPRINT de fase I / II para explorar los posibles beneficios del selumetinib en pacientes pediátricos con neurofibroma plexiforme (NP) inoperable relacionado con NF1. Los ensayos clínicos de Koselugo&en pacientes adultos con NF1-NP y un ensayo de formulación apropiada para la edad para pacientes pediátricos están planificados para comenzar este año.