
Contacto:Error Zhou (Señor.)
Teléfono: más 86-551-65523315
Móvil/WhatsApp: más 86 17705606359
QQ:196299583
Skype:lucytoday@hotmail.com
Correo electrónico:sales@homesunshinepharma.com
Agregar:1002, Huanmao edificio, Nº 105, Mengcheng camino, hefei ciudad, 230061, Porcelana
Apellis Pharma es líder en el desarrollo de terapias dirigidas C3, dedicadas al desarrollo de terapias pioneras y las mejores en su clase a través de métodos innovadores dirigidos A3 para el tratamiento de una amplia gama de medicamentos impulsados por enfermedades no controladas o sobreactivación de la cascada del complemento, incluidas las de los campos de la hematología, la oftalmología y la nefrología.
Recientemente, la compañía anunció que ha recibido comentarios formales por escrito de la Administración de Alimentos y Medicamentos de los Estados Unidos (FDA), fortaleciendo aún más la presentación de la inyección intravítrea de pegcetacoplan para el tratamiento de la degeneración macular relacionada con la edad (DMAE) y la atrofia geográfica secundaria (GA) del plan de solicitud de nuevo medicamento (NDA). El NDA estará respaldado por los datos de eficacia y seguridad del estudio DERBY y OAKS de Fase 3 y el estudio FILLY de Fase 2.
En comentarios escritos, la FDA declaró que si los ensayos clínicos son adecuados y están bien controlados, la agencia no distinguirá entre las diferentes fases del ensayo, y los tres estudios parecen ser adecuados y bien controlados. Sobre la base de estos comentarios, todavía se espera que Apellis presente el NDA en la primera mitad de 2022, y cree que no se requiere investigación adicional para presentar el NDA.
El director médico de Apellis, Federico Grossi, MD, dijo: "Estamos muy contentos de que los comentarios de la FDA sean consistentes con nuestro plan. Planeamos presentar un NDA pegcetacoplan basado en los datos de más de 1,500 pacientes en 3 estudios aleatorios y bien controlados. GA. Es una enfermedad devastadora que causa ceguera. Esperamos trabajar estrechamente con la FDA para llevar el primer tratamiento a la población de pacientes de GA".
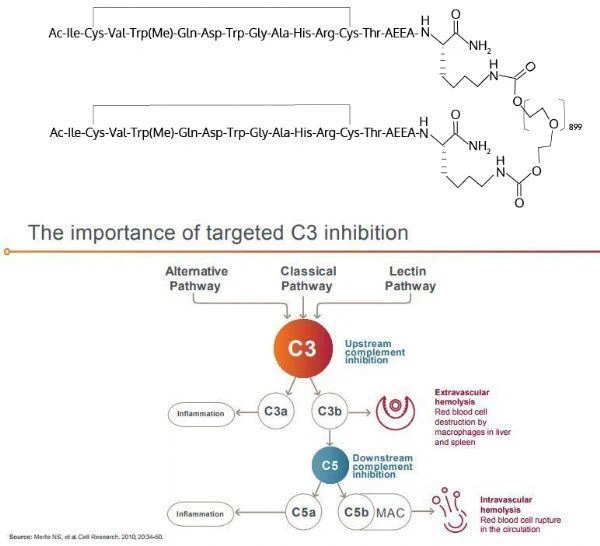
Características estructurales y mecanismo del pegcetacoplan
La AG es un tipo avanzado de degeneración macular relacionada con la edad (DMAE), y la DMAE es la principal causa de ceguera. La enfermedad de AG afecta a la parte central de la retina, la mácula, que es responsable de la visión central. La sobreactivación del complemento conduce a un crecimiento patológico irreversible en la AG, y C3 es el único objetivo para el control preciso de la sobreactivación del complemento. La AG es progresiva e irreversible, lo que lleva a daño central de la visión y pérdida permanente de la visión. Según la investigación publicada, hay más de 5 millones de pacientes con AG en todo el mundo y alrededor de 1 millón en los Estados Unidos. Actualmente, no existe un tratamiento aprobado para la AG.
Pegcetacoplan es un inhibidor C3 dirigido diseñado para regular la activación excesiva de la cascada del complemento. La cascada del complemento es una parte del sistema inmunológico humano, y su activación excesiva es la causa de la aparición y el desarrollo de muchas enfermedades graves. Pegcetacoplan es un péptido cíclico sintético que se une a un polímero de polietilenglicol y se une específicamente a C3 y C3b. Actualmente, pegcetacoplan se está desarrollando para tratar una variedad de enfermedades, que incluyen: atrofia geográfica (GA), hemoglobinuria paroxística nocturna (HPN) y glomerulopatía C3. En los Estados Unidos, la FDA ha otorgado a pegcetacoplan la calificación de vía rápida para el tratamiento de PNH y GA.
En mayo de 2021, Empaveli (pegcetacoplan) fue aprobado por la FDA de los Estados Unidos para el tratamiento de pacientes adultos con hemoglobinuria paroxística nocturna (HPN). Empaveli fue aprobado a través del proceso de revisión prioritaria, que tiene el potencial de mejorar los estándares de atención de la HPN y redefinir el tratamiento de la HPN.
Vale la pena mencionar que Empaveli es la primera y única terapia dirigida C3 que ha recibido la aprobación regulatoria. Este medicamento es adecuado para: (1) pacientes adultos con HPN que no han recibido tratamiento previamente; (2) Inhibidores de C5 previamente recibidos Pacientes adultos con HPN de Soliris (eculizumab) y Ultomiris (ravulizumab).
En la última década más o menos, la única opción para el tratamiento de la HPN eran los inhibidores de C5, pero muchos pacientes todavía experimentan hipohemoglobinosis persistente, que a menudo conduce a fatiga debilitante y transfusiones de sangre frecuentes. En los ensayos clínicos, Empaveli puede proporcionar un amplio control de la HPN, mejorando la vida de los pacientes con HPN al aumentar los niveles de hemoglobina y reducir la necesidad de transfusiones de sangre.