
Contacto:Error Zhou (Señor.)
Teléfono: más 86-551-65523315
Móvil/WhatsApp: más 86 17705606359
QQ:196299583
Skype:lucytoday@hotmail.com
Correo electrónico:sales@homesunshinepharma.com
Agregar:1002, Huanmao edificio, Nº 105, Mengcheng camino, hefei ciudad, 230061, Porcelana
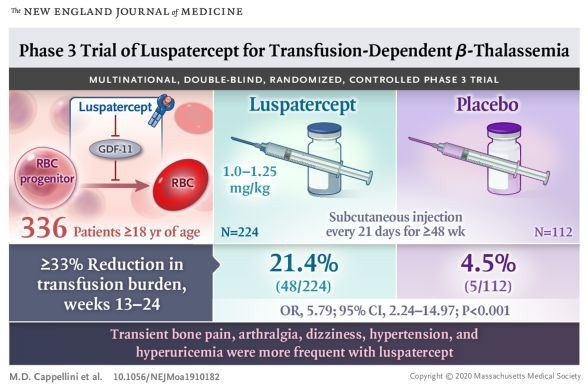
Bristol-Myers Squibb (BMS) y Acceleron Pharmaceuticals han anunciado recientemente que los resultados del estudio clave Fase III CREEN que evalúa el agente de maduración de glóbulos rojos Reblozyl (luspatercept) en el tratamiento de la beta talasemia se ha publicado en la principal revista médica internacional&"; New England Journal of Medicine GG"; (NEJM)). El título del artículo es: Un ensayo de fase 3 de luspatercept en pacientes con talasemia β dependiente de la transfusión.
Los resultados mostraron que los pacientes en el grupo de tratamiento con Reblozyl tuvieron una carga significativamente menor de transfusión de sangre en comparación con el grupo placebo. Según los resultados de este estudio, Reblozyl fue aprobado por la FDA de los EE. UU. En noviembre 2019 para el tratamiento de la anemia en pacientes adultos con beta talasemia que requieren una infusión regular de glóbulos rojos.
Reblozyl es el primer medicamento aprobado por la FDA para tratar la anemia relacionada con la beta talasemia, y es el primer y único agente de maduración de glóbulos rojos aprobado por la FDA, que representa una nueva clase de terapia que ayuda a los pacientes a reducir los glóbulos rojos regulando la etapa tardía de maduración de glóbulos rojos Carga de infusión. Cabe señalar que Reblozyl no es adecuado como sustituto de la infusión de glóbulos rojos en pacientes que necesitan corregir la anemia de inmediato.
BELIEVE es un estudio aleatorizado, doble ciego, controlado con placebo, multicéntrico realizado en pacientes adultos con talasemia β dependiente de transfusión que requieren transfusión regular de glóbulos rojos (6-20 unidades de transfusión de glóbulos rojos cada 24 semanas , Y durante este período, ningún período de transfusión de sangre no excede 35 días). En el estudio, los pacientes fueron asignados aleatoriamente para recibir Reblozyl combinado con el mejor tratamiento de soporte (BSC) o placebo en combinación con BSC. En este estudio, BSC incluyó: infusión de glóbulos rojos, medicamentos quelantes de hierro, antibióticos, antivirales, tratamiento antimicótico y / o soporte nutricional según sea necesario.
Los resultados mostraron que durante las 1 {{{1 3}} - {{1 5}} 4 semanas, la proporción de pacientes cuya carga de transfusión de glóbulos rojos se redujo por> ; {{1}}% (al menos {{{1 5}}}} unidades) desde el nivel basal fue significativamente mayor en el grupo de tratamiento con Reblozyl que en el grupo de placebo, llegando al estudio&# {{{{1 3}}}}; punto final primario de s. Además, el estudio también cumplió con todos los puntos finales secundarios clave: pacientes con una reducción en la carga de transfusión de eritrocitos> {{1}}}% durante las semanas {{1 3}} {{{{ 1 4}}}} - 49, pacientes con una reducción en la carga de transfusión de eritrocitos> {{{{1 {{2 2}}}}} }% durante las semanas 1 {{1 3}} - {{1 5}} 4 o {{1 3}} {{{{{{19} } 4}}}} - 4 {{2 1}} En proporción, el grupo de tratamiento con Reblozyl fue significativamente más alto que el grupo placebo. En este estudio, los eventos adversos más comunes (de cualquier grado) en el grupo de tratamiento con Reblozyl fueron más de 5% mayores que en el grupo de placebo: dolor óseo ({{1 0}}. { {{{1 4}}}}% vs {{1 {{1 5}}}}. {{1 3}}%), mareos ( {{1 4}}. {{1 5}}% vs {{1 {{1 {{2 2} }}}}}. {{1 {{2 2}}}}%), e hipertensión ({{1 {{1 5 }}}}. 1% vs {{1 5}}. {{2 1}}%), hiperuricemia ({{{{1 4}} }}. {{1 5}}% vs 0%).
El ingrediente farmacéutico activo de Reblozyl&# 39 es luspatercept, que es el primer agente de maduración de glóbulos rojos (EMA) que regula la maduración de los glóbulos rojos tardíos. El medicamento es una proteína de fusión soluble. El dominio Fc de la IgG humana 1 se fusiona con el dominio extracelular del receptor de tipo activina IIB (ActRIIB). Como trampa de ligando, puede regular la maduración tardía de los glóbulos rojos a través de la unión dirigida. El ligando específico de la superfamilia del factor de crecimiento transformante (TGF) -β reduce la activación de la vía de señalización Smad 2 / 3 , mejora la generación de glóbulos rojos ineficaces, promueve la maduración de la sangre roja tardía células, y aumenta los niveles de hemoglobina.
Luspatercept fue desarrollado globalmente por Shinki (adquirido por BMS) en cooperación con Acceleron Pharmaceuticals. Actualmente, las partes también están evaluando el potencial de luspatercept para el tratamiento de los agentes estimulantes de la eritropoyesis (ESA), pacientes con SMD de bajo riesgo (estudio de COMANDOS de Fase III), beta talasemia sin transfusión (estudio de Fase II MÁS ALLÁ) y mielofibrosis. La industria también es muy optimista sobre las perspectivas comerciales de Luspatercept' A fines del año pasado, EvaluatePharma lanzó el informe&"; Vantage 2019 Preview GG"; que contaba con el 20 amplificador R&más valioso; D proyectos en el mundo. Luspatercept clasificó 18 th con un valor presente neto (VPN) de US $ 3. 1 mil millones.

En la actualidad, Reblozyl' es otra solicitud de licencia de productos biológicos (BLA) para el tratamiento del síndrome mielodisplásico (SMD) que está siendo revisada por la FDA. RS) y requieren una infusión de glóbulos rojos (RBC) para pacientes adultos con anemia por síndrome de mielodisplásico (MDS) de riesgo muy bajo a riesgo moderado. La fecha objetivo del método de tarifa de usuario de medicamentos recetados (PDUFA) es el 4, 2020 de abril.
Anteriormente, analistas del famoso banco de inversión de Wall Street Jefferies señalaron que si la FDA también aprueba la anemia por síndrome mielodisplásico (MDS), el pico de ventas anuales de Reblozyl&# 39 alcanzará 2 mil millones de dólares. dolares